
این شیمیدان بسیاری از ایدههای اولیه درباره تفکیک یونی در محلولها را فرمولبندی کرد . مدلی جدید برای اسید و باز ارایه داد . جایزه نوبل شیمی سال 1903 را برد . رابطه بین انرژی فعالسازی و سرعت واکنشهای شیمیایی را فرمولبندی کرد . رابطهای را بین مقدار کربن دی اکسید موجود در هواکره و دمای کره زمین پیشنهاد کرد ؛ پدیدهای که امروز به نام اثر گلخانهای شناخته شدهاست و . ...
سوانت اگوست آرنیوس (Svante August Arrhenius) در سال 1859 در ویک ، شهری نزدیک اوپسالا در سوئد متولد شد . پدرش ، نقشهبردار زمین در دانشگاه اوپسالا بود که بعدها به مقام سرپرستی نیز رسید . در اوان کودکی ، در کنار پدرش با انبوه محاسبات ریاضی آشنا شد . در دبیرستان به استعداد ریاضیات و فیزیک خود پی برد و در سال 1876 به عنوان جوانترین و قابلترین دانشآموز فارغالتحصیل شد . سپس وارد دانشگاه اوپسالا شد اما از آنجا راضی نبود و به انستیتو فیزیک آکادمی علمی سوئد در استکهلم رفت . در آنجا زیر نظر اریک ادلاند بر روی هدایت الکتریکی الکترولیتها کار کرد و در سال 1884 مدرک دکترایش را در همین زمینه گرفت . هر چند که اساتیدش به پایاننامه او نمره خوبی ندادند اما همین پایاننامه او را به جایزه نوبل شیمی سال 1903 رساند .
وی در مهمترین قسمت این پایاننامه اظهار داشت که نه نمک خالص و نه آب خالص ، هیچکدام به تنهایی رسانای الکتریکی نیستند ، اما محلول این دو ماده رساناست . دلیل این امر را هم تفکیک نمک به ذرات باردار ، که بعدها توسط مایکل فارادی « یون » نامیده شدند ، دانست . فارادی اعتقاد داشت که یونها در حضور جریان الکتریکی شکل میگیرند اما آرنیوس معتقد بود که در غیاب جریان الکتریکی نیز محلول نمکها دارای یون میباشد . همین امر باعث بروز چالشی بزرگ در جمع دانشمندان الکتروشیمی از جمله فارادی ، کلازیوس ، اسوالد و وانتهوف گردید .
وی در سال 1884 تعریف جدیدی از اسید و باز ارایه کرد که در این تعریف ، اسید مادهای بود که در محلول آبیاش یون هیدروژن تولید میکند و باز مادهای است که در محلول آبیاش یون هیدروکسید تولید میکند .
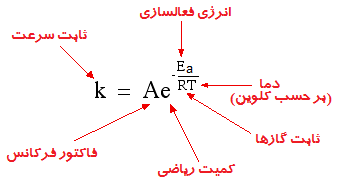
در سال 1889 مفهوم انرژی فعالسازی واکنش را ارایه داد . معادله آرنیوس ، ارتباط کمّی بین انرژی فعالسازی و سرعت واکنش شیمیایی نشان میدهد :
آرنیوس در سال 1902 پژوهشهای زیستفیزیکی خود را آغاز کرد . او مشخص کرد که واکنشهای شیمیایی صورت گرفته در اندامهای زنده ، از همان قوانین واکنشهای انجامشده در لولههای آزمایش پیروی میکنند . در سال 1904 در دانشگاه کالیفرنیا دورهای را درباره کاربرد روشهای شیمیفیزیکی در مطالعه تئوری سمّیت و ضدسمّیت گذراند که نتیجه آن در سال 1907 تحت عنوان « ایمنیشناسی در شیمی » منتشر شد .
وی بعدها به وادی زمینشناسی (دوران یخبندان) ، ستارهشناسی و کهکشانشناسی فیزیکی وارد شد و در مورد منشا تولد منظومه خورشیدی پژوهشهایی را انجام داد . وی همچنین ایده « زبان جهانی » را ، که نوعی زبان انگلیسی اصلاحشده بود ، را مطرح کرد .
آرنیوس تلاش کرد تا به اثر تغییر غلظت کربندیاکسید را بر روی تغییرات دمای سطح زمین محاسبه کند ؛ پدیدهای که امروز به آن « اثر گلخانهای » گفته میشود . وی که از کارهای فوریه و تیندال الهام میگرفت ، معادله ریاضی این پدیده را به صورت زیر ارایه داد :
ΔF=a ln(C/C0)
که در این معادله C غلظت گاز کربندیاکسید بر حسب ppmv و C0 غلظت استاندارد (پایه) کربندیاکسید ، ΔF تابش نفوذی ( اختلاف انرژی تابشی جذب شده و بازتابانده شده توسط زمین) بر حسب وات بر متر مربع است . ثابت آلفا (α) نیز عددی بین 5 تا 7 است . بدین ترتیب ، آرنیوس اولین کسی بودهاست که تاثیر افزایش غلظت گاز CO2 بر اثر سوختن سوختهای فسیلی را بر گرمایش زمین پیشبینی کردهاست .
سوانت آرنیوس در سال 1927 به دلیل التهاب رودهای حاد در اوپسالا درگذشت . وی یکی از بنیانگذاران شیمیفیزیک است . معادله آرنیوس ، مدل اسید- باز آرنیوس ، گودال ماه آرنیوس و آزمایشگاههای آرنیوس ، مواردی است که پس از مرگش ، به پاس زحمات او نامگذاری شدهاند .آرنیوس در سالهای عمر خود موفق به دریافت جوایز و مدالهای متعددی گردید که مهمترین آنها عبارتند از :
1- مدال دیوی 1902 2- جایزه نوبل شیمی 1903
3- جایزه ویلارد گیبس 4- مدال فرانکلین
منبع: شیمی دانشی برای همه روزگاران





